近日,欧盟委员会正式发布法规(EU) 2023/464文件,修订了法规(EC) No 440/2008的附件,该附件是作为REACH法规配套的测试方法。此次更新,引入了大量的最新的OECD体外测试方法以及移除了不少旧的测试方法,诸如两代生殖毒性试验(OECD 416)和UDS试验 (OECD486),有力推动了体外测试方法在欧盟的应用。根据本次更新,结合REACH法规测试要求,对本次涉及到的毒理学测试方法重要的变化进行总结:
1. 严重眼损伤/眼刺激
正式引入OECD 467-严重眼损伤和眼刺激的确定方法,采用该方法后,可以采用体外方法即可对物质做出合适的分类,大部分情况下无需引入体内方法。下图仅显示OECD 467方法中的一种测试策略,实际测试过程中,需要根据物质的液体/固体,水溶解性以及表面张力情况,主要通过OECD 492+OECD437,结合水溶解度、蒸汽压、表面张力、正辛醇水分配系数等理化性质,可以做出非此类/类别1/类别2的区分。或者通过OECD491+OECD437的组合,做出非此类/类别1/类别2的区分。
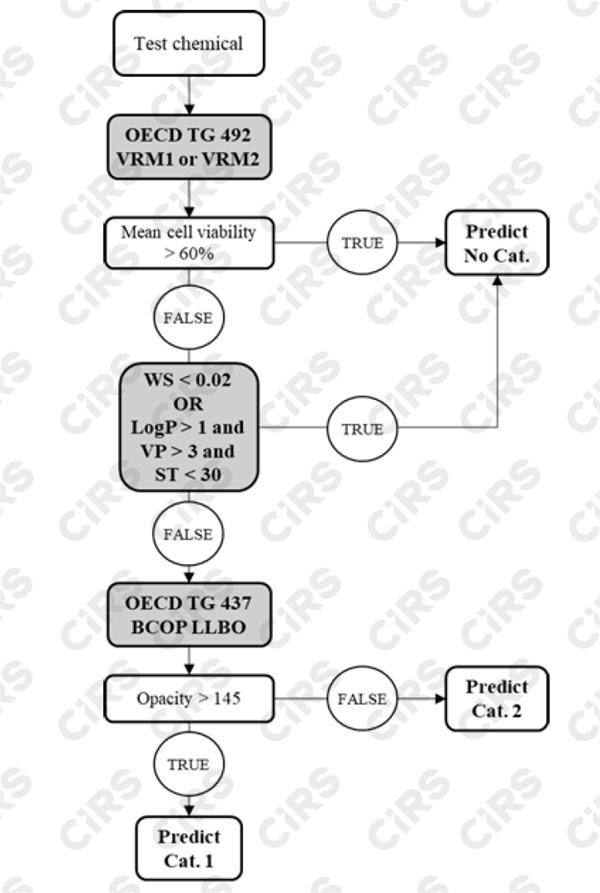
2. 皮肤致敏性
正式引入了OECD497-皮肤致敏性的确定方法,通过2个体外实验方法(OECD 442C+OECD 442E)再加一个QSAR结果,如果体外实验结果比较理想,结合QSAR结果,即可根据下图做出合适的分类,如果体外实验结果或者QSAR结果不太理想,也有一定可能性对物质完成皮肤致敏性分类,通过这些方法可以有效降低LLNA的测试需求。
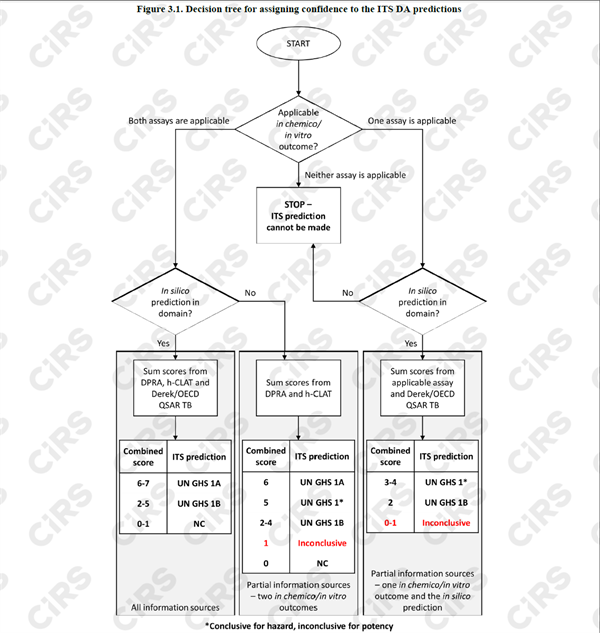
3. 致突变性
正式引入两种比较新的体内基因方法,包括OECD 488-转基因啮齿动物体细胞和生殖细胞基因突变以及OECD 470-哺乳动物红细胞Pig-a基因突变测定,也给体内基因突变的实验设计更多选择。同时移除了UDS方法,目前在欧洲REACH法规卷宗评估要求开展的体内基因突变实验中,基本上会要求在Comet或转基因方法2选1。
4. 生殖毒性/发育毒性
正式移除两代生殖毒性试验(OECD 416),统一用扩展一代生殖毒性试验(OECD 443)代替,早在之前的REACH法规要求里,就已经统一用OECD 443取代了,由于该实验费用高昂,有欧洲实验室报价高达100万欧元,对面临卷宗评估的高吨位注册人造成巨大压力。
5. 内分泌干扰特性
新增若干新的内分泌干扰特性体外方法,比如OECD 455-利用稳定转染细胞系检测雌激素受体激动剂的体外转录激活试验、OECD456-R295R细胞系类固醇生成试验、OECD 45-利用稳定转染细胞系检测雄激素受体激动剂的体外转录激活试验以及OECD493-人重组雌激素受体亲和力体外试验等。体内方法包括OECD 440-啮齿类动物子宫增重试验(UT试验)和OECD441-大鼠中的Hershberger试验(H试验)。由于目前欧盟CLP法规已完成修订,正式引入内分泌干扰特性分类,预计未来内分泌干扰试验有可能成为考察物质特性的一个重要组成部分。
涉及到其他毒理,生态毒理的试验方法由于不是常见的测试方法,对试验的选择影响不大,所以就不一一赘述了。
专家点评:
此次测试方法的更新,可以看到欧盟在推进体外测试方法,尤其是皮肤腐蚀/刺激,严重眼损伤/刺激以及皮肤致敏性方面是全球领先的,这些体外测试的方法应用也将逐步扩展到其他国家的化学品登记注册中,从而更好推动全球替代方法的应用。同时我们也注意到近期欧盟在更新CLP法规,新引入内分泌干扰特性分类,此次内分泌干扰特性的体外和体内测试方法的公布,有可能未来成为研究物质相关内分泌干扰特性的试验组合,需要引起企业关注。
新加入的体内基因突变测试方法包括OECD 488和OECD 470,也给企业更多的试验选择,但由于这些方法比较新,包括价格方面也相对较高,导致实验室的选择面临较大困难,也对实验室提出了更高的要求。两代生殖毒性测试,在较早的环节里已经被扩展一代生殖毒性测试所取代,对欧盟REACH注册的影响已经不存在,对于要开展相关测试的注册人经济压力较大(OECD 443单项测试费用相当高)。
综上所述,企业在开展REACH注册要求的相关节点时,应根据最新的指南,结合合适的方法,从而避免测试不满足相关法规要求。
相关推荐:
